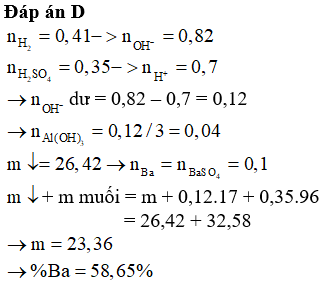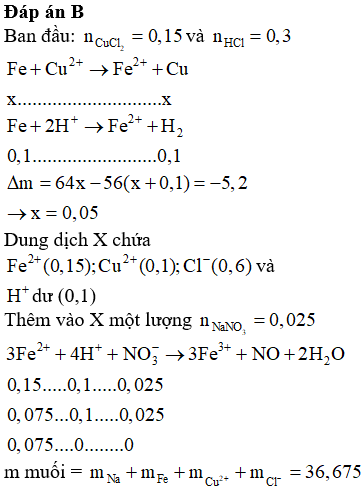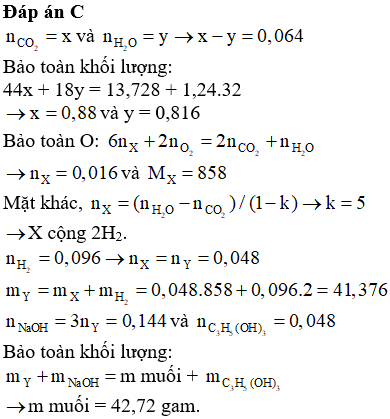30 đề thi THPT Quốc gia môn Hóa năm 2022 có lời giải (Đề số 26)
-
45514 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
 Xem đáp án
Xem đáp án
Đáp án D
Hg có nhiệt độ nóng chảy thấp nhất vì là KL duy nhất ở trạng thái lỏng
Câu 2:
Kim loại nào tác dụng với N2 ở nhiệt độ thường?
 Xem đáp án
Xem đáp án
Đáp án C
Li tác dụng được với N2 ở điều kiện thường tạo hợp chất Li3N
Câu 3:
Tính chất hoá học chung của kim loại là
 Xem đáp án
Xem đáp án
Đáp án B
Tính chất hóa học đặc trưng của kim loại là tính khử (dễ bị oxi hóa)
Câu 5:
Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, ánh kim, dẻo) được gây nên chủ yếu bởi
 Xem đáp án
Xem đáp án
Đáp án D
Tính chất vật lý chung của KL là do các e tự do trong cấu trúc mạng tinh thể KL gây ra
Câu 6:
Dãy gồm các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3 đặc, nguội là:
 Xem đáp án
Xem đáp án
Đáp án C
Al, Fe, Cr bị thụ động hóa trong HNO3 đặc nguội
Câu 7:
Chất nào sau đây không phải là chất lưỡng tính?
 Xem đáp án
Xem đáp án
Đáp án C
Al là kim loại tác dụng với axit, bazơ nhưng không mang tính lưỡng tính
Câu 8:
Diêm tiêu kali được dùng để chế tạo thuốc nổ đen, đồng thời được dùng làm phân bón. Công thức hóa học của diêm tiêu kali là
 Xem đáp án
Xem đáp án
Đáp án C
Diêm tiêu kali là KNO3
Câu 9:
Sự hình thành thạch nhũ trong các hang động đá vôi là do phản ứng hoá học nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Xem phần hợp chất kim loại kiềm thổ (sgk 12)
Câu 10:
Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng một lượng dư kim loại sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Cu + 2Fe3+ → Cu2+ + 2Fe2+
Câu 11:
Phương trình hóa học nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án A
A sai vì Cr tác dụng với H2SO4 loãng tạo CrSO4
Câu 12:
Quá trình nào sau đây không gây ô nhiễm môi trường không khí?
 Xem đáp án
Xem đáp án
Đáp án C
Quang hợp của cây xanh tạo O2 nên không làm ô nhiễm môi trường
Câu 13:
Các este thường có mùi thơm dễ chịu: isoamyl axetat có mùi chuối chín, etyl butirat có mùi dứa chín, etyl isovalerat có mùi táo, ... Este có mùi chuối có công thức cấu tạo thu gọn là:
 Xem đáp án
Xem đáp án
Đáp án C
CH3COOCH2CH2CH(CH3)2 là este tạo mùi thơm chuối chín
Câu 14:
Từ dầu thực vật (chất béo lỏng) làm thế nào để có được bơ (chất béo rắn)
 Xem đáp án
Xem đáp án
Đáp án C
Chất béo lỏng(không no) cộng H2 sẽ trở thành chất béo rắn (no)
Câu 15:
Công thức nào sau đây là của xenlulozơ?
 Xem đáp án
Xem đáp án
Đáp án A
Xenlulozơ có CTCT là [C6H7O2(OH)3]n
Câu 16:
X là hợp chất hữu cơ vừa tác dụng với dung dịch AgNO3/NH3, vừa tác dụng với dung dịch NaOH nhưng không làm quỳ tím đổi màu. Vậy X là
 Xem đáp án
Xem đáp án
Đáp án C
HCOOCH3 vừa tác dụng với AgNO3/NH3 vừa tác dụng với NaOH nhưng không làm đổi màu quì tím
Câu 17:
Mùi tanh của cá (đặc biệt là cá mè) chủ yếu do chất (CH3)3N có tên gọi nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án D
(CH3)3N là trimetyl amin
Câu 18:
Polietilen là chất dẻo mềm, được dùng nhiều để làm
 Xem đáp án
Xem đáp án
Đáp án A
Xem phần ứng dụng của một số polime (sgk 12)
Câu 20:
Chất nào không tác dụng với dung dịch AgNO3/NH3
 Xem đáp án
Xem đáp án
Đáp án B
Các ankin có liên kết ba đầu mạch sẽ tham gia được phản ứng với AgNO3/NH3 tạo được kết tủa vàng
Câu 21:
Cho phản ứng sau: aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O. Các hệ số a, b, c, d, e là những số nguyên đơn giản nhất. Tổng (a + b) bằng
 Xem đáp án
Xem đáp án
Đáp án C
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Câu 22:
Chất X có công thức phân tử C3H6O2, là este của axit axetic. Công thức cấu tạo thu gọn của X là
 Xem đáp án
Xem đáp án
Đáp án A
C3H6O2 là este của axit axetic (CH3COOH) nên có CT CH3COOCH3
Câu 23:
Hoà tan hoàn toàn m gam Al vào dung dịch HNO3 rất loãng, thu được hỗn hợp gồm 0,015 mol khí NO2 và 0,01 mol khí NO (phản ứng không tạo NH4NO3). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Bảo toàn electron:
Câu 24:
Cho kim loại Fe lần lượt phản ứng với dung dịch các chất riêng biệt sau: H2SO4 loãng, CuCl2, Fe(NO3)2, AgNO3, NaCl. Số trường hợp có phản ứng hóa học xảy ra là
 Xem đáp án
Xem đáp án
Đáp án D
Có 3 trường hợp xảy ra phản ứng:
Fe + H2SO4 loãng → FeSO4 + H2
Fe + CuCl2 → FeCl2 + Cu
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Câu 25:
Hòa tan 32 gam hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lít khí NO (đktc). Khối lượng CuO trong hỗn hợp ban đầu là
 Xem đáp án
Xem đáp án
Đáp án A
Bảo toàn electron: 2nCu = 3nNO
Câu 26:
Cho tất cả các đồng phân đơn chức, mạch hở, có cùng công thức phân tử C2H4O2 lần lượt tác dụng với: K, KOH, KHCO3. Số phản ứng xảy ra là
 Xem đáp án
Xem đáp án
Đáp án B
Các đồng phân đơn chức, mạch hở, có cùng công thức phân tử C2H4O2 gồm CH3COOH và HCOOCH3.
Có 4 phản ứng
CH3COOH + Na → CH3COONa + H2
CH3COOH + NaOH → CH3COONa + H2O
CH3COOH + Na2CO3 → CH3COONa + CO2 + H2O
HCOOCH3 + NaOH → HCOONa + CH3OH
Câu 27:
Nhận định sai là
 Xem đáp án
Xem đáp án
Đáp án B
Saccarozơ và glixerol đều tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam
Câu 28:
Cho 500 ml dung dịch glucozơ phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 10,8 gam Ag. Nồng độ của dung dịch glucozơ đã dùng là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 29:
Cho 15,00 gam glyxin vào 300 ml dung dịch HCl, thu được dung dịch X. Cho X tác dụng vừa đủ với 250 ml dung dịch KOH 2M, thu được dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
Dung dịch Y chứa:
NH2-CH2-COO-: 0,2
Bảo toàn điện tích
m rắn = 44,95
Câu 30:
Cho các poline sau: polietilen, tinh bột, tơ tằm, xenlulozơ triaxetat, polibutađien, sợi len. Số polime thiên nhiên là
 Xem đáp án
Xem đáp án
Đáp án A
Polime tự nhiên gồm: tinh bột, tơ tằm, sợi len
Câu 32:
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(2) Cho dung dịch HCl tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(3) Sục khí H2S vào dung dịch FeCl2.
(4) Sục khí NH3 tới dư vào dung dịch AlCl3.
(5) Sục khí CO2 tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(6) Cho dung dịch Na2CO3 vào dung dịch Ba(HCO3)2.
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
 Xem đáp án
Xem đáp án
Đáp án C
(1) NaOH + Ca(HCO3)2 → CaCO3 + Na2CO3 + H2O
(2) HCl dư + NaAlO2 → NaCl + AlCl3 + H2O
(3) Không phản ứng.
(4) NH3 + H2O + AlCl3 → Al(OH)3 + NH4Cl
(5) CO2 + H2O + NaAlO2 → Al(OH)3 + NaHCO3
(6) Na2CO3 + Ba(HCO3)2 → BaCO3 + 2NaHCO3
Câu 34:
Cho các phát biểu sau:
(a) Dung dịch lòng trắng trứng có phản ứng màu biure.
(b) Amino axit là chất rắn kết tinh, dễ tan trong nước.
(c) Dung dịch phenol không làm đổi màu quỳ tím.
(d) Hiđro hóa hoàn toàn triolein (xúc tác Ni, t°) thu được tristearin.
(e) Fructozơ là đồng phân của glucozơ.
(f) Amilozơ có cấu trúc mạch phân nhánh.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án C
Chỉ có (6) sai, amilozơ mạch không nhánh.
Câu 40:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào ống nghiệm 2 – 3 giọt CuSO4 5% và 1 ml dung dịch NaOH 10%. Lắc nhẹ, gạn bỏ phần dung dịch. Lấy kết tủa cho vào ống nghiệm (1).
Bước 2: Rót 2 ml dung dịch saccarozơ 5% vào ống nghiệm (2) và rót tiếp vào đó 0,5 ml dung dịch H2SO4 loãng. Đun nóng dung dịch trong 3 – 5 phút.
Bước 3: Để nguội dung dịch, cho từ từ NaHCO3 tinh thể vào ống nghiệm (2) và khuấy đều bằng đũa thủy tinh cho đến khi ngừng thoát khí CO2.
Bước 4: Rót dung dịch trong ống (2) vào ống (1), lắc đều cho đến khi tủa tan hoàn toàn.
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án B
A. Sai, thêm Ba(OH)2 loãng làm tăng thể tích (làm loãng sản phẩm thủy phân), mặt khác dung dịch vẩn đục nên mất thời gian đợi lắng hoặc lọc.
C. Sai, thu được dung dịch xanh thẫm.
D. Sai, các chất tham gia và sản phẩm đều tan tốt nên không tách lớp.